
תוכן עניינים:
- מְחַבֵּר Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- שונה לאחרונה 2025-01-22 16:59.
צעדים
- מצא את המספר האטומי של האטום שלך.
- קבע את המטען של האטום.
- שנן את הרשימה הבסיסית של האורביטלים.
- להבין סימון תצורת אלקטרונים.
- שנן את סדר האורביטלים.
- מלא את האורביטלים לפי מספר האלקטרונים באטום שלך.
- השתמש בטבלה המחזורית כקיצור דרך חזותי.
באופן דומה, מהם השלבים לכתיבת תצורת אלקטרונים?
צעדים
- מצא את המספר האטומי של האטום שלך.
- קבע את המטען של האטום.
- שנן את הרשימה הבסיסית של האורביטלים.
- להבין סימון תצורת אלקטרונים.
- שנן את סדר האורביטלים.
- מלא את האורביטלים לפי מספר האלקטרונים באטום שלך.
- השתמש בטבלה המחזורית כקיצור דרך חזותי.
שנית, מה זה Subshell? א subshell היא תת-חלוקה של קליפות אלקטרונים המופרדות על ידי אורביטלים של אלקטרונים. קונכיות משנה מסומנים s, p, d ו-f בתצורת אלקטרונים.
באופן דומה, נשאל, מהו שלטון האנד?
כלל האנד . שלטון האנד : כל מסלול בתת-קליפה תפוס יחיד עם אלקטרון אחד לפני שאורביטל אחד תפוס כפול, ולכל האלקטרונים באורביטלים תפוסים בודדים יש את אותו ספין.
כמה אלקטרונים יש בכל קליפה?
כל קליפה יכולה להכיל רק מספר קבוע של אלקטרונים: הקליפה הראשונה יכולה להחזיק עד שני אלקטרונים , הקליפה השנייה יכולה להכיל עד שמונה (2 + 6) אלקטרונים, הקליפה השלישית יכולה להחזיק עד 18 (2 + 6 + 10) וכן הלאה. הנוסחה הכללית היא שהקליפה ה-n' יכולה באופן עקרוני להחזיק עד 2(n2) אלקטרונים.
מוּמלָץ:
איך תצורת האלקטרונים קשורה למספרים קוונטיים?
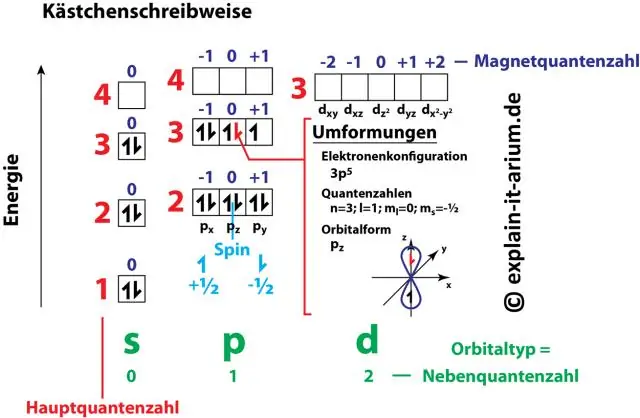
צמדי המספרים והאותיות בתצורת אלקטרונים מייצגים שניים מארבעת המספרים הקוונטיים של האלקטרון. המספרים הקוונטיים הללו מספרים לנו מידע נוסף על תכונות האלקטרונים והאורביטלים שלהם. המספר הקוונטי העיקרי (n) אומר לנו את רמת האנרגיה של האלקטרון ואת גודלו
לאיזה יסוד יש תצורת אלקטרונים 2 5?

איור 5.9 החץ מציג דרך שנייה לזכור את הסדר שבו תתמלאות רמות. טבלה 5.2 מציגה את תצורות האלקטרונים של היסודות עם המספרים האטומיים 1 עד 18. יסוד מספר אטומי תצורת אלקטרונים גופרית 16 1s22s22p63s23p4 כלור 17 1s22s22p63s23p5 ארגון 18 1s623s22s22s
איך משרטטים משוואה שלב אחר שלב?
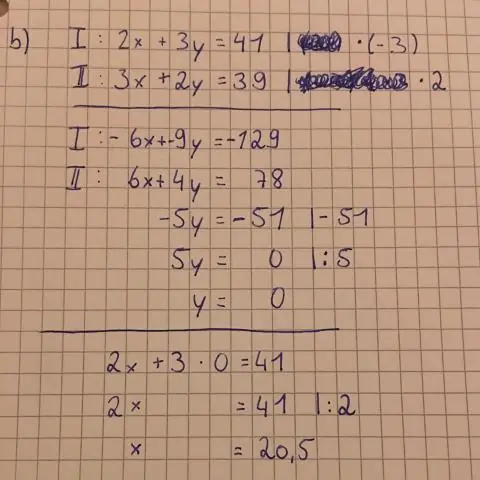
הנה כמה שלבים שצריך לבצע: חבר את x = 0 למשוואה ופתור עבור y. שרטט את הנקודה (0,y) על ציר ה-y. חבר את y = 0 למשוואה ופתור את x. שרטט את הנקודה (x,0) על ציר ה-x. צייר קו ישר בין שתי הנקודות
איזו תצורת אלקטרונים מייצגת אטום במצב היסוד שלו?

אז כל תצורת אלקטרונים שבה האלקטרון האחרון (שוב, אלקטרון הערכיות) נמצא במסלול אנרגיה גבוה יותר, אומרים שהאלמנט הזה נמצא במצב נרגש. לדוגמה, אם נסתכל על מצב הקרקע (אלקטרונים במסלול הזמין הנמוך ביותר מבחינה אנרגטית) של חמצן, תצורת האלקטרונים היא 1s22s22p4
איך עושים מדרון צעד אחר צעד?

ישנם שלושה שלבים בחישוב השיפוע של קו ישר כאשר לא ניתנת לך המשוואה שלו. שלב ראשון: זהה שתי נקודות על הקו. שלב שני: בחר אחד להיות (x1, y1) והשני להיות (x2, y2). שלב שלישי: השתמש במשוואת השיפוע כדי לחשב את השיפוע
