- מְחַבֵּר Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- שונה לאחרונה 2025-01-22 16:59.
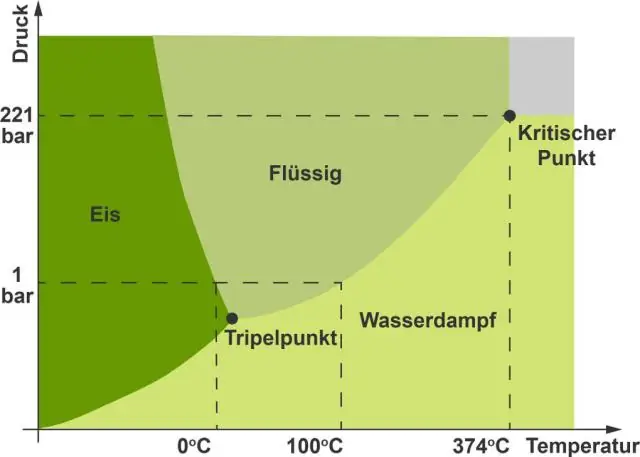
ב דיאגרמת המים , ה מִדרוֹן של הקו בין המצב המוצק לנוזל הוא שלילי במקום חיובי. הסיבה היא מים הוא חומר יוצא דופן בכך שמצבו המוצק פחות צפוף מהמצב הנוזלי.
כתוצאה מכך, מדוע שיפוע עקומת ההיתוך שלילי למים?
ה עקומת התכה אוֹ עקומת היתוך של קרח/ מים הוא מאוד מיוחד. יש לזה שיפוע שלילי בשל העובדה שכאשר הקרח נמס, הנפח הטוחני יורד. קרח למעשה נמס בטמפרטורה נמוכה יותר בלחץ גבוה יותר.
כמו כן, מהי המטרה של דיאגרמת פאזות? א דיאגרמת פאזות בכימיה פיזיקלית, הנדסה, מינרלוגיה ומדעי החומרים הוא סוג של תרשים המשמש להצגת תנאים (לחץ, טמפרטורה, נפח וכו') שבהם נבדלים מבחינה תרמודינמית שלבים (כגון מצבים מוצקים, נוזליים או גזים) מתרחשים ומתקיימים במקביל ב שִׁוּוּי מִשׁקָל.
דעו גם, מה ייחודי בתרשים הפאזות של מים?
דיאגרמות שלבים הם גרפים עם טמפרטורה על ציר אחד ולחץ על ציר אחר. הם מחולקים למקטעים שמציינים באיזה מצב נמצא חומר בלחצים וטמפרטורות מסוימות. מים הוא הוגן ייחודי כי קו ההיתוך שלו משתפל שמאלה. רוב החומרים האחרים משתפלים ימינה.
איזה שלב הם מים ב-1 אטמוספירה ו-0 מעלות צלזיוס?
בטמפרטורות ולחצים אופייניים על כדור הארץ (מסומן ב-E למטה) מים הוא נוזל, אבל הוא הופך למוצק (כלומר, קרח) אם הטמפרטורה שלו יורדת למטה 0 ° ג וגזי (כלומר, מים אדים) אם הטמפרטורה שלו עולה מעל 100 מעלות ג , באותו לחץ.
מוּמלָץ:
איך יודעים אם שינוי פאזה חיובי או שלילי?
אם הסטת הפאזה היא אפס, העקומה מתחילה במקור, אך היא יכולה לנוע שמאלה או ימינה בהתאם להזזת הפאזה. שינוי פאזה שלילי מצביע על תנועה ימינה, והיסט פאזה חיובי מציין תנועה שמאלה
מדוע שורש הקובייה של מספר שלילי הוא מספר שלילי?

שורש קובייה של מספר שלילי תמיד יהיה שלילי מכיוון שקוביות של מספר פירושו העלאתו לחזקה שלישית - שהיא אי זוגית - גם שורשי הקוביות של מספרים שליליים חייבים להיות שליליים. כאשר המתג כבוי (כחול), התוצאה שלילית. כאשר המתג פועל (צהוב), התוצאה חיובית
מדוע למים יש נקודת התכה גבוהה?
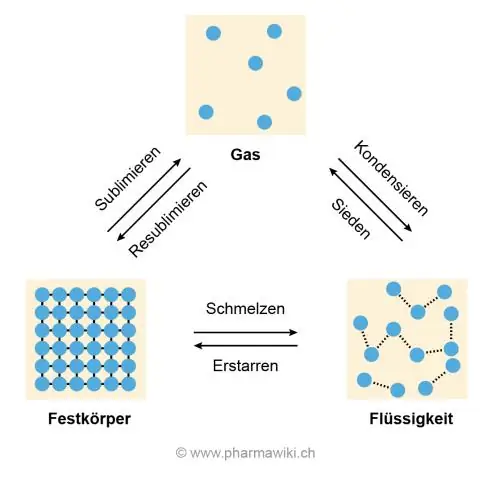
הסיבה לטמפרטורות ההיתוך והרתיחה הגבוהות היא קשר המימן בין מולקולות מים שגורם להן להיצמד זו לזו ולהתנגד להיפרדות, מה שקורה כאשר קרח נמס ומים רותחים והופכים לגז
מדוע אנו משתמשים במיקרוסקופ ניגודיות פאזה?

ניגודיות פאזה היא ללא ספק השיטה הנפוצה ביותר במיקרוסקופ אור ביולוגי. זוהי טכניקת מיקרוסקופיה מבוססת בתרבית תאים והדמיית תאים חיים. בעת שימוש בטכניקה זולה זו, ניתן לראות תאים חיים במצבם הטבעי ללא קיבוע או תיוג קודם
מדוע למים יש נקודת רתיחה גבוהה והתכה?

הסיבה לטמפרטורות ההיתוך והרתיחה הגבוהות היא קשר המימן בין מולקולות מים שגורם להן להיצמד זו לזו ולהתנגד להיפרדות, מה שקורה כאשר קרח נמס ומים רותחים והופכים לגז
