
- מְחַבֵּר Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- שונה לאחרונה 2025-01-22 16:59.
אם העקומה עוברת עם כיוון השעון, ה תְצוּרָה הוא R; אם העקומה עוברת נגד כיוון השעון, ה תְצוּרָה הוא S. כדי לקבל את התחליף העדיפות מספר ארבע בחלק העליון של הקרנת פישר , עליך להשתמש באחד משני המהלכים המותרים בתרשים השני.
השאלה היא גם איך אתה מקצה תצורת R ו-S?
לאחר שכל התחליפים שלך תועדפו בצורה הנכונה, אתה יכול כעת לתת שם/תווית למולקולה ר אוֹ ס . שים את התחליף בעדיפות הנמוכה ביותר מאחור (קו מקווקו). קבע אם הכיוון מ-1 ל-2 עד 3 בכיוון השעון או נגד כיוון השעון.
אפשר גם לשאול, איך אתה יכול לדעת אם הקרנת פישר היא כיראלית? להכין הקרנת פישר , אתה צופה א כיראל במרכז כך ששני תחליפים יוצאים אליך מהמטוס, ושני תחליפים חוזרים למישור, כפי שמוצג כאן. אז ה כיראל מרכז הופך לצלב על הקרנת פישר . כל צלב על א הקרנת פישר הוא כיראל מֶרְכָּז.
באופן דומה, איך עוברים מהקרנת פישר לקו איגרות חוב?
כדי להמיר את הקרנת פישר אל א קו אג"ח נוסחה אתה פשוט מצייר זיג-זג קַו של שישה אטומי פחמן. אז אתה שם קבוצת אלדהיד בקבוצות C-1 ו-OH על כל אחד מחמשת אטומי הפחמן האחרים. שימו לב שה- קו אג"ח הנוסחה אינה נותנת מידע סטריאוכימי.
מה ההבדל בין אננטיומרים לדיאסטראומרים?
ישנם שני סוגים של סטריאואיזומרים- אננטיומרים ודיאסטראומרים . אננטיומרים לְהַכִיל כיראל מרכזים שהם תמונות מראה ואינם ניתנים להשפעה על גבי. דיאסטראומרים לְהַכִיל כיראל מרכזים שאינם ניתנים להשפעה על גבי אך אינם תמונות מראה. יכולים להיות הרבה יותר מ-2 בהתאם למספר הסטריאומרכזים.
מוּמלָץ:
איך תצורת האלקטרונים קשורה למספרים קוונטיים?
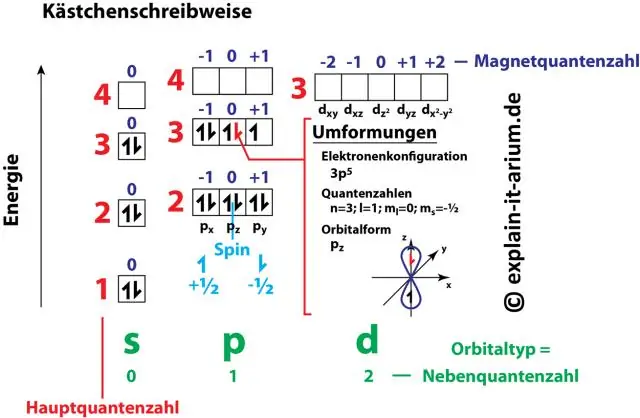
צמדי המספרים והאותיות בתצורת אלקטרונים מייצגים שניים מארבעת המספרים הקוונטיים של האלקטרון. המספרים הקוונטיים הללו מספרים לנו מידע נוסף על תכונות האלקטרונים והאורביטלים שלהם. המספר הקוונטי העיקרי (n) אומר לנו את רמת האנרגיה של האלקטרון ואת גודלו
איך כותבים את תצורת האלקטרונים עבור MN?

למנגן, לעומת זאת, יש תצורת אלקטרונים של 1s22s22p63s23p64s23d5 ותצורת גז אצילי של [Ar]4s23d5, וכתוצאה מכך אלקטרון אחד לא מזווג בכל תת-אורביטל תלת מימדי
איך אתה יודע אם תצורת R או S שלו?

מכיוון שהאטום הרביעי בעדיפות הגבוהה ביותר ממוקם מאחור, החץ צריך להראות כאילו הוא עובר על פני שעון. אם הוא הולך בכיוון השעון, אז זה אננטיומר R; אם הוא הולך נגד כיוון השעון, זהו אננטיומר S
איך מוצאים את תצורת האלקטרונים לחמצן?

בכתיבת תצורת האלקטרונים עבור חמצן, שני האלקטרונים הראשונים יעברו במסלול 1s. מכיוון ש-1s יכול להחזיק רק שני אלקטרונים, שני האלקטרונים הבאים עבור O עוברים במסלול של 2s. ארבעת האלקטרונים הנותרים יעברו במסלול 2p. לכן תצורת האלקטרון O תהיה 1s22s22p4
איך עושים תצורת אלקטרונים צעד אחר צעד?

שלבים מצא את המספר האטומי של האטום שלך. קבע את המטען של האטום. שנן את הרשימה הבסיסית של האורביטלים. להבין סימון תצורת אלקטרונים. שנן את סדר האורביטלים. מלא את האורביטלים לפי מספר האלקטרונים באטום שלך. השתמש בטבלה המחזורית כקיצור דרך חזותי
