
- מְחַבֵּר Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- שונה לאחרונה 2025-01-22 16:58.
ה המסה האטומית הממוצעת של יסוד הוא הסכום של ה המונים מהאיזוטופים שלו, כל אחד מוכפל בשפע הטבעי שלו (העשרוני הקשור לאחוז של אטומים של זה אֵלֵמֶנט שהם מאיזוטופ נתון). מסה אטומית ממוצעת = ו1M1 + ו2M2 +…
לאחר מכן, אפשר גם לשאול, כיצד מחושבת המסה האטומית של יסוד?
ל לחשב ה מסה אטומית של סינגל אָטוֹם של אֵלֵמֶנט , חבר את ה מסה של פרוטונים וניוטרונים. דוגמה: מצא את מסה אטומית של איזוטופ של פחמן שיש בו 7 נויטרונים. אתה יכול לראות מהטבלה המחזורית שלפחמן יש א אָטוֹמִי מספר של 6, שהוא מספר הפרוטונים שלו.
יתר על כן, האם המסה האטומית זהה למשקל האטומי? מסה אטומית (Mא) האם ה מסה של אָטוֹם . בודד אָטוֹם יש מספר מוגדר של פרוטונים וניטרונים, אז ה מסה הוא חד משמעי (לא ישתנה) והוא סכום מספר הפרוטונים והנייטרונים אָטוֹם . משקל אטומי הוא ממוצע משוקלל של מסה מכל ה אטומים של יסוד, המבוסס על שפע האיזוטופים.
בדרך זו, איך מחשבים את המסה האטומית הממוצעת של פחמן?
ל למצוא ה מסה אטומית ממוצעת , אתה לוקח מספר מסוים של אטומים , למצוא סך הכל מסה של כל איזוטופ, ולאחר מכן מחלקים את הסכום הכולל מסה מכל ה אטומים לפי המספר הכולל של אטומים . נניח שיש לך, נניח, 10,000 אטומים שֶׁל פַּחמָן . אז יש לך 9893 אטומים של 12C ו-107 אטומים של 13C.
מהי המסה האטומית הממוצעת של טיטניום על פני כדור הארץ?
איזוטופ: 46Ti שפע: 75.200% מסה : 45.95263 איזוטופ אמו: 48Ti שפע: 12.300% מסה : 47.94795 איזוטופ אמו: 50Ti שפע: 12.500% מסה : 49.94479 אמו.
מוּמלָץ:
איך מחשבים את המסה האטומית הממוצעת של סטרונציום?

אז, אנו מחשבים אותו על ידי לקיחת המסה המשוקללת של כל אחד מהאיזוטופים וחיבורם יחד. אז, עבור המסה הראשונה, נכפיל 0.50% מ-84 (אמו - יחידות מסה אטומית) = 0.042 אמו, ונוסיף את זה ל-9.9% מ-86 אמו = 8.51 אמו, וכן הלאה
כיצד נקבעת המסה האטומית הממוצעת בטבלה המחזורית?

המסה האטומית הממוצעת של יסוד מחושבת על ידי סיכום מסות האיזוטופים של היסוד, כל אחד מהם מוכפל בשפע הטבעי שלו על פני כדור הארץ. כאשר עושים חישובי מסה כלשהם הכוללים יסודות או תרכובות, השתמש תמיד במסה אטומית ממוצעת, אותה ניתן למצוא בטבלה המחזורית
איך מחשבים את המסה האטומית של בורון?
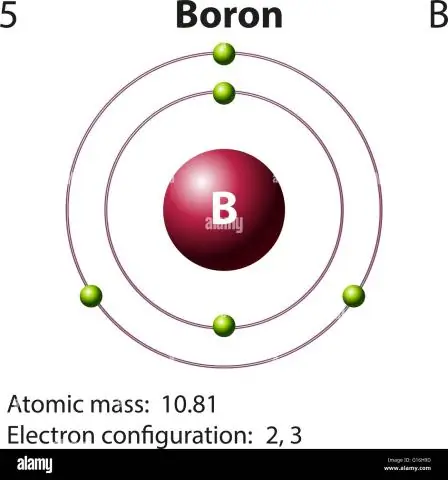
עבור בורון, משוואה זו תיראה כך: 5 פרוטונים + 5 נויטרונים = 10 יחידות מסה אטומית (AMU) או, עבור איזוטופ הבור הנפוץ יותר (כ-5 פרוטונים + 6 נויטרונים = 11 AMU)
מהי המסה הממוצעת המשוקללת?

המסה האטומית של יסוד היא הממוצע המשוקלל של מסות האיזוטופים של יסוד. ניתן לחשב את המסה האטומית של יסוד בתנאי שהכמות היחסית של האיזוטופים המופיעים באופן טבעי של היסוד והמסה של אותם איזוטופים ידועים
לאיזה יסוד יש את המסה האטומית הגדולה ביותר?

Ununoctium הוא היסוד הכבד ביותר, אבל הוא מעשה ידי אדם. היסוד הכבד ביותר המתרחש באופן טבעי הוא אורניום (מספר אטומי 92, משקל אטומי 238.0289)
