
- מְחַבֵּר Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- שונה לאחרונה 2025-01-22 16:59.
אז, אנחנו לחשב זה על ידי לקיחת המשוקלל מסה של כל אחד מהאיזוטופים וחיבורם יחד. אז, לראשון מסה , נכפיל 0.50% מ-84 (amu - מסה אטומית יחידות) = 0.042 אמו, והוסיפו אותו ל-9.9% מ-86 אמו = 8.51 אמו, וכן הלאה.
בהמשך, אפשר גם לשאול, איך מחשבים את המסה האטומית הממוצעת?
חישוב מסה אטומית ממוצעת ה מסה אטומית ממוצעת של אלמנט הוא הסכום של המונים מהאיזוטופים שלו, כל אחד מוכפל בשפע הטבעי שלו (העשרוני הקשור לאחוז של אטומים של אותו יסוד שהם מאיזוטופ נתון). מסה אטומית ממוצעת = ו1M1 + ו2M2 +…
דעו גם, אילו שלושה סוגי מידע דרושים כדי לחשב מסה אטומית ממוצעת? מספר האיזוטופים הקיימים עבור האלמנט. ה אָטוֹמִי מספר עבור האלמנט. אחוז השפע של כל איזוטופ.
אפשר גם לשאול, מהו הערך הקרוב ביותר למסה האטומית של סטרונציום?
סטרונציום . בדו ח שלה משנת 1961 המליצה הוועדה על אר(Sr) = 87.62 מבוסס על מסה -קביעה ספקטרומטרית של ניר. זֶה ערך תוקן ל-Aר(Sr) = 87.62(1) בשנת 1969 והוא נותר ללא שינוי מאז.
מה יש מסה של 1 אמו?
יחידת מסה אטומית (מסומלת AMU או amu) מוגדרת כ-1/12 במדויק מהמסה של אטום של פחמן-12. לאטום פחמן-12 (C-12) יש שישה פרוטונים ושש נויטרונים בגרעין שלו. במונחים לא מדויקים, AMU אחד הוא הממוצע של פּרוֹטוֹן מסת מנוחה ואת נֵיטרוֹן מסת מנוחה.
מוּמלָץ:
מהי המסה האטומית הממוצעת של אטום?

המסה האטומית הממוצעת של יסוד היא סכום המסות של האיזוטופים שלו, כל אחד מוכפל בשפע הטבעי שלו (העשרוני הקשור לאחוז האטומים של אותו יסוד שהם של איזוטופ נתון). מסה אטומית ממוצעת = f1M1 + f2M2 +
כיצד נקבעת המסה האטומית הממוצעת בטבלה המחזורית?

המסה האטומית הממוצעת של יסוד מחושבת על ידי סיכום מסות האיזוטופים של היסוד, כל אחד מהם מוכפל בשפע הטבעי שלו על פני כדור הארץ. כאשר עושים חישובי מסה כלשהם הכוללים יסודות או תרכובות, השתמש תמיד במסה אטומית ממוצעת, אותה ניתן למצוא בטבלה המחזורית
איך מחשבים את המסה האטומית של בורון?
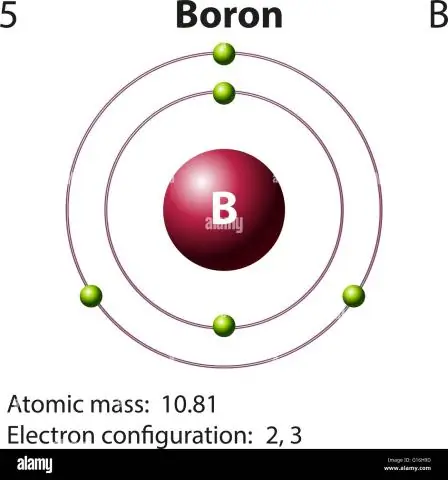
עבור בורון, משוואה זו תיראה כך: 5 פרוטונים + 5 נויטרונים = 10 יחידות מסה אטומית (AMU) או, עבור איזוטופ הבור הנפוץ יותר (כ-5 פרוטונים + 6 נויטרונים = 11 AMU)
מהי המסה הממוצעת המשוקללת?

המסה האטומית של יסוד היא הממוצע המשוקלל של מסות האיזוטופים של יסוד. ניתן לחשב את המסה האטומית של יסוד בתנאי שהכמות היחסית של האיזוטופים המופיעים באופן טבעי של היסוד והמסה של אותם איזוטופים ידועים
לאיזה יסוד יש את המסה האטומית הגדולה ביותר?

Ununoctium הוא היסוד הכבד ביותר, אבל הוא מעשה ידי אדם. היסוד הכבד ביותר המתרחש באופן טבעי הוא אורניום (מספר אטומי 92, משקל אטומי 238.0289)
